Cell Rep:暨南大学曹广超等团队合作发现高脂肪饮食引起炎症性肠病的潜在新机理
时间:2024-08-28 18:00:34 热度:37.1℃ 作者:网络
炎症性肠病(IBD)在西方国家发病率很高。西方饮食中的高脂肪含量是导致这种发病的主要原因之一;然而,其潜在机制尚未完全确定。
2024年8月16日,暨南大学曹广超、何蓉蓉、李怡芳、孙万阳、尹芝南、中山大学郅敏共同通讯在Cell Reports 在线发表题为“Inherent preference for polyunsaturated fatty acids instigates ferroptosis of Treg cells that aggravates high-fat-diet-related colitis”的研究论文,该研究中发现高脂饮食(HFD)会诱导肠道调节性T(Treg)细胞的铁死亡,这可能是破坏免疫耐受和发展结肠炎的关键启动步骤。
与效应T细胞相比,Treg细胞更倾向于脂质代谢,并且更喜欢多不饱和脂肪酸(PUFA)来合成膜磷脂。因此,食用含有大量花生四烯酸等PUFA的HFD会培养易受脂质过氧化和铁死亡影响的脆弱Treg。Treg细胞特异性缺乏GPX4,GPX4是维持细胞氧化还原稳态和预防铁死亡的关键酶,会显著加剧HFD诱导的IBD的发病机制。总的来说,这些研究扩展了我们对IBD病因的理解。
炎症性肠病(IBD)是一种以令人衰弱的慢性复发性炎症和严重的上皮功能障碍为特征的疾病。由于环境和生活方式的快速变化,近年来IBD的患病率不断上升,并已成为一个世界性的健康问题。IBD的病因尚未完全明确,涉及饮食、遗传、感染和免疫系统等多种因素之间的相互作用。在饮食因素中,高脂饮食(HFD)被广泛认为与IBD的发展有着密切的相关性。虽然西方饮食与IBD风险之间联系的确切机制尚未完全确定,但已经提出了一些看似合理的机制。具体而言,西方饮食与肠道菌群和上皮屏障功能的变化有关,从而引发促炎环境。
多种免疫细胞群参与触发IBD中的促炎环境。相反,调节性T细胞(Treg)始终表达高水平的FOXP3和CD25,具有免疫抑制功能,对限制IBD的免疫耐受至关重要。先前的研究表明,HFD会导致结肠和小肠中的免疫细胞激活,CD4+ Foxp3+ Tregs显着减少。减少的Treg细胞无法限制促炎性免疫反应,从而加剧IBD的发展。但HFD治疗后Treg细胞减少的机制仍不清楚。
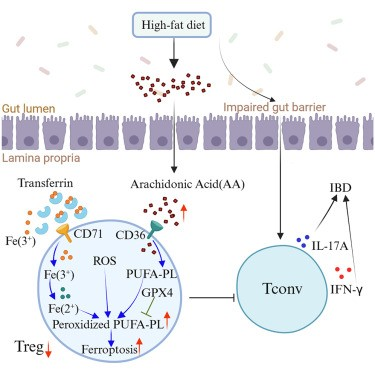
图形摘要(图源自Cell Reports )
与传统的效应T细胞相比,Treg细胞有利于脂质氧化来代谢和获取能量,从而产生更高水平的活性氧(ROS)。ROS是膜多不饱和脂肪酸(PUFA)过氧化损伤导致细胞铁死亡的危险因素,这种独特的细胞死亡方式受多种细胞代谢事件的调控,包括线粒体活性、氧化还原稳态以及铁、氨基酸、脂质和糖的代谢。谷胱甘肽过氧化物酶4(GPX4)是维持细胞氧化还原稳态和防止铁死亡的关键酶,它以谷胱甘肽(GSH)为辅助因子还原膜磷脂氢过氧化物,花生四烯酸(AA)及其酯化产物是脂质过氧化的主要底物,是诱导铁死亡的关键。西方饮食中富含AA等PUFA,已知它们会引发铁死亡并加重结肠炎。这项研究的目的是探索HFD相关结肠炎的病因。作者假设西方饮食中AA或其代谢前体的高水平以及Treg对脂质代谢的内在偏好可能导致铁死亡,而这种免疫抑制细胞群的减少可能会破坏肠粘膜的免疫耐受,从而引发结肠炎。
在这项研究中,作者发现Treg细胞倾向于脂质代谢,并倾向于使用PUFA来合成磷脂。食用含有高水平AA及其前体等PUFA的HFD会培养易受脂质过氧化和铁死亡影响的脆弱Treg细胞。由于HFD还会诱发肠道菌群失调,增加肠道屏障的通透性,从而触发常驻免疫细胞的激活。激活后的剧烈氧化还原代谢会产生高水平的ROS,引发脂质过氧化和Treg细胞的铁死亡,从而破坏免疫耐受并增加结肠炎的风险。作者还发现HFD治疗后结肠Treg细胞中的GPX4减少,而删除Treg细胞中的Gpx4会进一步加剧其铁死亡并加重HFD诱导的肠道炎症。补充α-生育酚可以逆转Treg的铁死亡并显著改善HFD诱导的结肠炎。总之,作者的工作扩展了作者对IBD病因的理解,确定了Treg细胞在控制免疫平衡方面的潜在靶点,并为预防西方饮食相关性结肠炎提供了一种有希望的方法。
参考消息:
https://www.cell.com/cell-reports/fulltext/S2211-1247(24)00986-0


