Lancet子刊:中国医学科学院杨仁池团队发现治疗原发性免疫性血小板减少症的潜在新方法
时间:2023-04-12 20:28:46 热度:37.1℃ 作者:网络
脾酪氨酸激酶(Syk)抑制剂是原发性免疫性血小板减少症的一种治疗选择。该研究旨在评估sovleplenib(Syk抑制剂)在原发性免疫性血小板减少症患者中的安全性、耐受性、药代动力学、初步活性和推荐的2期剂量。
2023年4月4日,中国医学科学院/北京协和医学院杨仁池团队在Lancet Haematology在线发表了题为“Sovleplenib (HMPL-523), a novel Syk inhibitor, for patients with primary immune thrombocytopenia in China: a randomised, double-blind, placebo-controlled, phase 1b/2 study”的研究论文,该项随机、双盲、安慰剂对照、1b/2期研究评估了口服Syk抑制剂sovleplenib对中国原发性免疫性血小板减少症患者无应答或既往原发性免疫性血小板减少症治疗复发的疗效。剂量为100mg至400mg,每天1次,耐受性良好。300mg的sovleplenib观察到令人鼓舞的总体缓解率(16[80%]/ 20)和持久缓解率(8[40%])。在接受sovleplenib治疗的患者中,与治疗相关的腹泻和高血压的发生率为5%或更低。
该研究结果表明,solvleplenib对中国原发性免疫性血小板减少症患者具有良好的活性和安全性。该研究研究提供了证据,Syk抑制剂可能是对先前治疗反应不充分的原发性免疫性血小板减少症患者的有效治疗选择。该研究研究结果支持进一步研究sovelplenib在这一患者群体中的作用。

原发性免疫性血小板减少症是一种自身免疫性疾病,其特征是血小板破坏增加和产生受损,导致血小板计数低(小于100 × 10 9血小板/ L)。成人原发性免疫性血小板减少症的发病率为每100000人中2至5人。这种疾病的发病机制很复杂,尚不完全清楚。在这些机制中,Fcγ受体通过介导巨噬细胞吞噬引起血小板清除发挥关键作用。在原发性免疫性血小板减少症患者中,出血的迹象通常很轻微;然而,严重的低血小板计数(小于20 ×10 9血小板/ L)还是会与出血有关。
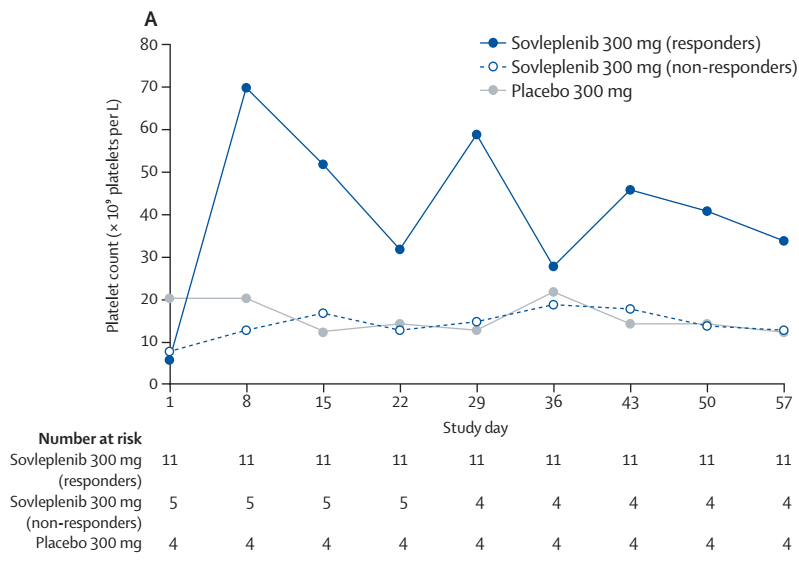
治疗期间不同组别患者血小板计数(图源自Lancet Haematology )
原发性免疫性血小板减少症的治疗策略主要集中在减少抗体产生、阻断血小板过早清除和增加血小板产生。对于血小板数低于30 × 109的患者,糖皮质激素被推荐作为一线治疗方式,这些患者没有症状或有轻微的活动性粘膜皮肤出血。虽然患者通常对一线治疗有反应,但大多数患者在停止使用糖皮质激素后复发,需要连续治疗。二线治疗包括使用促血小板生成素受体激动剂(如eltromopag和romiplostim)、生物制剂(如利妥昔单抗)和脾切除术,但对于一线治疗后的原发性免疫性血小板减少症的首选治疗方法尚无共识。
脾酪氨酸激酶(Syk)是一种免疫受体信号转导的调节因子,对B细胞活化和自身抗体的产生很重要,并在Fcγ受体介导的信号转导中起关键作用,包括细胞增殖、分化、存活、免疫调节和吞噬过程中的细胞骨架重排。Syk是原发性免疫性血小板减少症治疗的潜在靶点,可调节血小板破坏和产生之间的平衡。Fostamatinib是一种Syk抑制剂,于2018年被美国食品和药物管理局批准用于慢性原发性免疫性血小板减少症且对之前的治疗方案反应不充分的患者。然而,响应率很低,在两项3期临床试验的汇总分析中,101例患者中有43例(43%)有总体响应,18例(18%)有持续响应,并且先前的fostamatinib研究主要在白人人群中进行。因此,Syk抑制剂在中国原发性免疫性血小板减少症患者中的安全性和有效性尚不清楚。
Sovleplenib(也称为HMPL-523)是一种小分子、强效、选择性口服Syk抑制剂,在临床前研究(未发表)和临床研究中对B细胞淋巴瘤患者显示出较好的安全性和增加血小板计数的活性。该研究旨在评估sovleplenib在原发性免疫性血小板减少症患者中的安全性、耐受性、药代动力学、初步活性和推荐的2期剂量。
该项随机、双盲、安慰剂对照、1b/2期研究在中国9家医院进行。符合条件的患者年龄18-75岁,ECOG表现评分为0-1,原发性免疫性血小板减少症6个月以上,既往一线治疗无反应或复发,或反应不良或脾切除术后复发。剂量递增期(100mg、200mg或300mg,每天口服1次)和剂量扩大期(推荐2期剂量)分别为8周、双盲、安慰剂对照期,患者随机分配(3:1)接受sovleplenib或安慰剂,并采用交互式网络反应系统,随后是16周、开放标签期。在前8周,患者、研究人员和发起者对治疗分配情况进行了掩盖。主要疗效终点是在0-8周的连续两次随访中,血小板计数达到30 × 109(每升血小板数)或更高的患者比例,并且是基线的两倍,没有进行抢救治疗。该研究已在ClinicalTrials.gov注册,注册号为NCT03951623。
在2019年5月30日至2021年4月22日期间,对62名患者进行了资格评估,45名患者(73%)被随机分配。患者在8周双盲期间接受至少一剂研究药物(安慰剂[n=11]和sovleplenib 100mg [n=6]、200mg [n=6]、300mg [n=16]和400mg [n=6];该组是在观察到在以前的剂量下没有规程规定的安全事件后添加的)。所有参与者都是亚洲人;45例患者中男性18例(40%),女性27例(60%)。中位年龄为40∙0岁(IQR 33∙0 - 50∙0)。sovleplenib组34例患者中有10例(29%)与安慰剂组11例患者中5例(45%)同时接受抗原发性免疫性血小板减少治疗。2期推荐剂量为300mg,每天1次。
达到主要疗效终点的患者比例为100 mg组3例,200毫克组3例,300 mg组10例,400 mg组2例和安慰剂组1例。300mg组的总体缓解率为80%(20名持续接受sovelplenib的患者中有16名加上安慰剂的患者),在连续的sovleplenib 300 mg给药组持久缓解率为31% (15 / 16)和75%在0-24周内从安慰剂过渡到索夫普利尼。在28天的安全性评估期间,sovleplenib组发生了2个2级或更糟糕的治疗相关的紧急不良事件(高甘油三酯血症和贫血)。在0-8周期间,最常见的治疗突发不良事件是血乳酸脱氢酶、血尿和尿路感染的增加(sovelplenib组34例中有7例[21%],安慰剂组11例中有1例[9%]);隐血阳性和高尿酸血症(4例[12%]vs 3例[27%])。未记录致命的治疗突发不良事件。
该研究结果表明,Sovleplenib耐受性良好,推荐的2期剂量在原发性免疫性血小板减少症患者中显示出有希望的持久反应,这为未来的研究提供了证据。一项3期临床试验(NCT05029635)正在进行中,以确认sovleplenib对原发性免疫性血小板减少症患者的有效性和安全性。
原文链接:
https://www.thelancet.com/journals/lanhae/article/PIIS2352-3026(23)00034-0/fulltext#%20


