【Blood Cancer J】自体移植物中的克隆性浆细胞影响高危MM预后
时间:2023-05-09 11:30:16 热度:37.1℃ 作者:网络
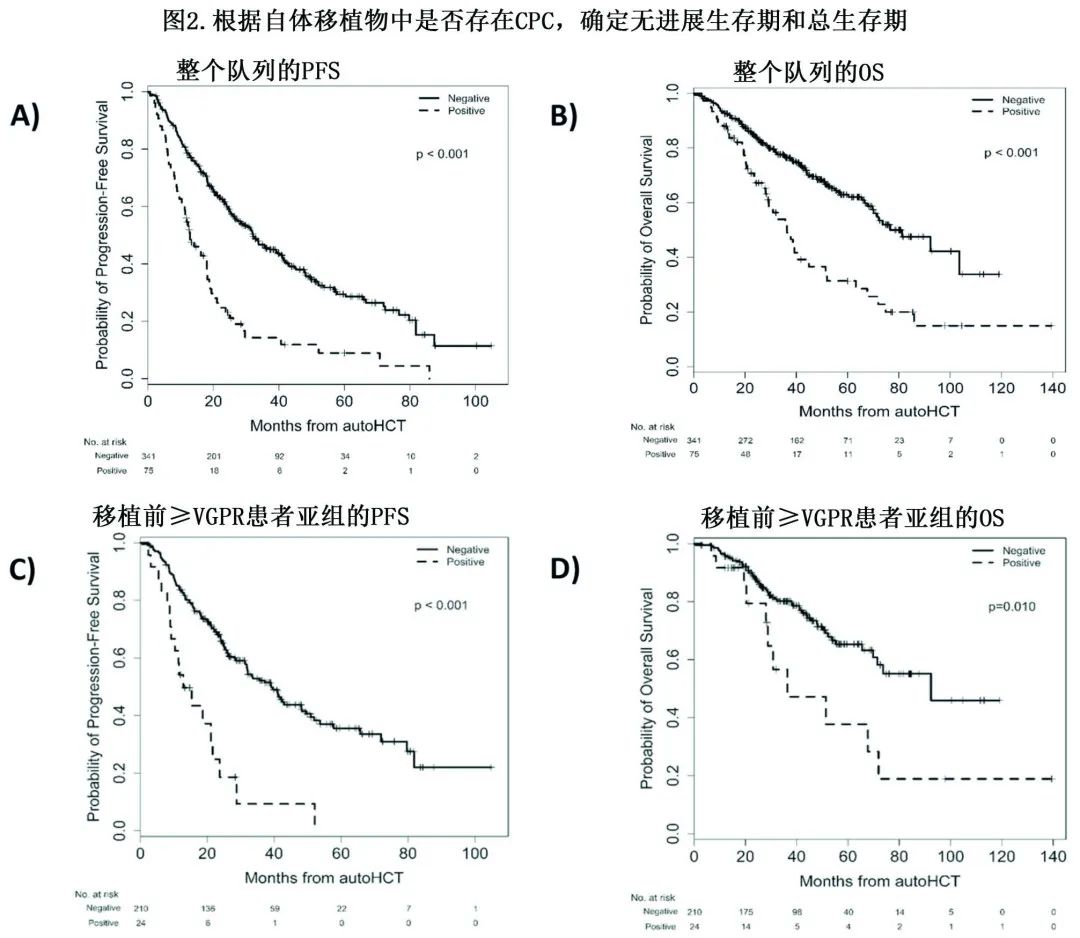
大剂量化疗和自体造血干细胞移植 (autoHCT)是多发性骨髓瘤 (MM) 患者一线治疗的标准方案,但与标危患者相比,具有高危细胞遗传学特征(HRMM)的患者在 autoHCT 后的结局较差。HRMM和标危MM患者的移植后3年无进展生存期 (PFS) 率分别为37%和49%,总生存期 (OS) 率分别为72%和85%。 在采集用于 autoHCT 的自体移植物(autografts)中,异常克隆性浆细胞 (aberrant clonal plasma cells,CPC) 的意义仍有争议。为评估接受 autoHCT 的 HRMM 患者中 MM 细胞污染自体移植物的影响,MD安德森癌症中心Muzaffar H. Qazilbash教授牵头一项纳入416例HRMM患者的单中心回顾性分析,结果证实自体移植物中 CPC 的存在和程度均可高度预测较差的 PFS 和 OS。研究结果近日发表于《Blood Cancer Journal》,该研究结果也登陆过2022年ASH会议Oral报告。 作者检索了其中心数据库中2008年至2018年间接受 autoHCT 的 HRMM 成人患者,对采集的单采产物进行6色二代流式细胞仪 (NGF) 检测CPC,灵敏度为0.001-0.003%。通过 NGF 将患者分为自体移植物中CPC+和 CPC-组。由于并非所有采集的自体移植物产品均在 autoHCT 时输注,并且对于同一患者,部分冻存袋可能是CPC+ 或CPC-,因此作者还评估了输注CPC+ 自体移植物对患者结局的影响。使用8色 NGF 评估骨髓样本中的 MRD 状态,灵敏度为1/10-5个细胞 (0.001%)。 使用FISH鉴定 del17p/TP53 缺失、t(4;14)/IGH::FGFR3、t(14;16)/IGH::MAF、1q21/CKS1B增益(CKS1B拷贝3个)或扩增(CKS1B拷贝≥4个)的高危细胞遗传学异常。 患者和疾病特征 416例 HRMM 患者纳入研究,中位年龄为62.4岁,57%为男性。75例 (18%)CPC+而341例 (82%) 为CPC-。CPC+ 组移植前接受VRD诱导方案的患者比例低于CPC-组 (24% vs.42%,p=0.004),但两组之间的诱导持续时间无差异 (p=0.37);CPC+组诱导后达到≥VGPR和 MRD 阴性的患者比例低于CPC-组(分别为32% vs. 62%;p<0.001和8% vs. 40%;p<0.001)。与 CPC-患者相比,CPC+患者的 Del[17p] 和1q+ 细胞遗传学异常显著更普遍(45% vs. 28%,p=0.007和68% vs. 45%,p<0.001)。此外两组之间使用的预处理方案无显著差异 (p=0.73)。根据自体移植物 CPC 状态分层的患者特征总结于表1。 结局 整个队列中位随访35.7个月。CPC+和CPC-组的100天和autoHCT 后最佳 CR 率分别为8% vs. 33% (p<0.001) 和19% vs. 54% (p<0.001)。CPC+组患者移植后 MRD 阴性 CR 的几率较低 (11% vs. 42%;p<0.001)。CPC+ vs.CPC-组中位PFS分别为12.8 vs. 32.1个月 (p<0.001),中位 OS 为36.4 vs. 81.2个月 (p<0.001)。 自体移植物CPC受累程度与移植后第100天的反应呈负相关:移植后第100天达到≥VGPR的患者的最大自体移植物 CPC 水平为0.02%,而达到≤PR的患者为1.04% (p=0.003)。同样,最大自体移植物CPC水平与移植后最佳反应呈负相关:达到≥VGPR的患者的平均最大自体移植物 CPC 水平为0.06%,而达到≤PR的患者为1.55% (p=0.004)。CPC+和CPC-组的移植前和移植后反应如图1所示。 评估整个患者队列时可发现,CPC+患者的 PFS(图2A,p<0.001)和OS(图2B,p<0.001)均明显更差。在 autoHCT 前达到≥VGPR的患者中,CPC+患者的 PFS [HR=3.38,p<0.001;图2C)和OS(HR=2.29,p=0.013;2D)较差;同样,autoHCT 前达到 MRD 阴性≥VGPR的患者中,CPC+患者的PFS (HR=4.21,p=0.006) 和OS (HR=7.04,p=0.002) 也劣于CPC-组。 在多变量分析 (MVA) 中,自体移植物中CPC阳性的程度可独立预测较差的PFS (HR=1.50;p=0.001) 和OS (HR=1.37;p=0.001);输注CPC+ 自体移植物产品可预测较差的PFS (HR=2.72;p<0.001)但 OS 并未显著较差 (HR=1.47];p=0.16)。与 ISS I 期相比,ISS II期和 III 期疾病的 MVA PFS 更差 [分别为HR=1.47,p=0.026) 和HR=1.55,P=0.014)]。HCT-CI 评分>3与 OS 较差相关 (HR=1.50;p=0.044),而移植后维持治疗与OS改善趋势相关 (HR=0.68;p=0.05)。PFS 和 OS 的 MVA 分别见表2和表3。在 CPC-和CPC+ 组中,autoHCT前和 autoHCT 后第100天的血液学缓解大部分保留了 PFS 和 OS 的统计学显著性,但在CPC+ 组内,autoHCT前的血液学反应并不能预测OS(p=0.60)。 在收集的自体移植物中,使用化疗进行干细胞动员不影响 CPC-的发生率,且与其他诱导治疗方案相比, VRD诱导治疗与PFS或OS改善均无关;在接受 VRD 诱导的患者亚组中,自体移植物 CPC 状态仍可高度预测PFS和OS。 由于研究的两个时间段使用不同的 CPC 检测方法,因此排除了早期移植的患者进行重复分析,并获得了相似的结果。 本研究是迄今为止评价 CPC 污染自体移植物对接受 autoHCT 的 MM 患者影响的最大研究,也是首次只关注 HRMM 患者。研究发现,在接受 autoHCT 的 HRMM 患者中,自体移植物中 CPC 的存在与较差的 PFS 和 OS 相关,且自体移植物 CPC 阳性的程度与较差的结局相关。通过MVA发现自体移植物 CPC 阳性与患者结局显著相关,这一结果在 autoHCT 前已达到≥VGPR或 MRD 阴性≥VGPR的患者中也同样存在。 总的来说,本研究显示自体移植物中 CPC 对 HRMM 自体 HCT 后结局有重大影响,自体移植物中 CPC 的存在和程度均可高度预测较差的 PFS 和OS,包括在 autoHCT 前达到≥VGPR和 MRD 阴性 CR/VGPR 的患者,而致力于清除 CPC 的新策略可改善患者结局。 参考文献 Oren Pasvolsky ,et al. Impact of clonal plasma cells in autografts on outcomes in high-risk multiple myeloma patients.Blood Cancer J . 2023 May 3;13(1):68. doi: 10.1038/s41408-023-00842-6.