Investigative Radiology:结合深度学习和放射组学实现自动且全面的全身MRI骨髓特征评估!
时间:2023-07-18 23:17:17 热度:37.1℃ 作者:网络
多发性骨髓瘤(MM)可累及整个骨骼系统,这对于分期、治疗反应评估和并发症评估带来了极大的困难。现代全身成像技术,如磁共振成像(MRI)或正电子发射断层扫描,可以评估完整的骨髓(BM),并且根据目前的指南对单克隆浆细胞疾病进行评估。由于时间限制,放射科医生通常只会报告BM病变的大致数量、少数示范性病变的大小、是否有骨折以及对肿瘤负荷是否增加、稳定或减少的总体印象。
然而,这种方法导致了从wb-MRI的数百万个体素到放射科医生报告的信息的巨大损失,这限制了影像学在临床决策和精确肿瘤学研究中的影响力。肿瘤负荷往往异质地分布在全身骨骼上,MM中也有空间基因组异质性的描述。
为了充分捕捉肿瘤疾病中骨髓病变的复杂性,并最大限度地利用成像数据集中的信息,需要一个新的概念来分析骨髓:首先,为每个骨髓空间(BMS)提取大量的特征,收集每个局部发现的信息,其次,将所有局部信息整合到整体的骨髓状态。为了将该系统应用于临床实践或大规模的研究数据集,这样的系统需要自动执行所有步骤。多发性骨髓瘤是一种散发性骨髓受累的典型疾病,大量的影像学特征,如病灶的大小、体积、强度和纹理以及弥漫性浸润。然而,即使在专门的肿瘤报告系统中,如MY-RADS22,报告中也只包括少数这样的高级影像特征。
 近日,发表在Investigative Radiology杂志的一项研究通过自动分割BM和随后对30个不同的BM空间(BMS)进行放射组学分析,实现从Wb-MRI自动、全面描述BM的概念。
近日,发表在Investigative Radiology杂志的一项研究通过自动分割BM和随后对30个不同的BM空间(BMS)进行放射组学分析,实现从Wb-MRI自动、全面描述BM的概念。
本项回顾性的多中心试验研究使用了来自8个中心的102名MM患者的总共106张wb-MRI图像进行评估。来自1号中心的50个wb-MRI用于训练分割算法(nnU-Nets)和放射组学算法,来自8个中心的56张wb-MRI用于独立测试。对来自90个wb-MRI的2700个BMS进行了人工分割,并用于分割算法的训练和测试。对于每个BMS,单独计算了296个放射组学特征。使用Dice评分来评估自动分割和人工参考分割之间的相似性。
使用多标签nnU-Net "分割算法对30个BMS进行分割,并对其进行单独标记;在来自中心1/中心2/中心3-8的独立测试集中,平均骰子得分达到0.88±0.06/0.87±0.06/0.83±0.11(放射科医生间的差异性,0.88±0.01)。来自多中心、多厂商测试集的子集(3-8中心)中,成像质量高、分割精度高(平均骰子得分,0.87),并与1中心的内部测试数据相当。对所有病人计算了由每个病人8880个描述性参数组成的放射组学BM表型,该表型是对30个BMS中的每一个的296个放射组学特征的计算结果。示范性病例显示了MM的典型骨髓模式与各自BMS的放射组学特征之间的相关性。在可信度测试中,基于放射组学BM表型模型的预测大小和体重与患者的实际大小和体重明显相关(分别为P = 0.002和P = 0.003)。
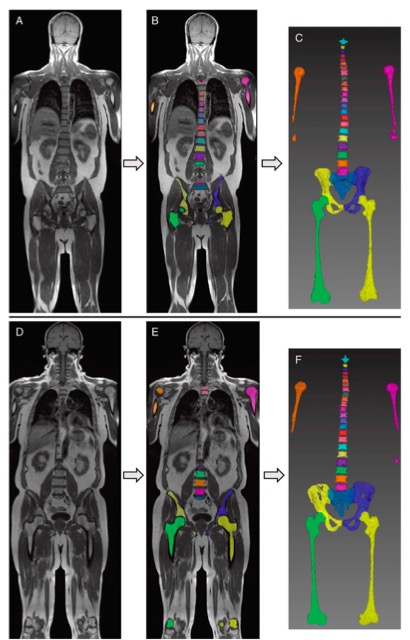
图 在外部测试集中由多标签lnnU-Net进行的全身骨髓自动分割。左侧显示的是冠状T1加权涡轮脊柱选择图像(A,D),中间显示的是由多标签lnnU-Net在该图像上提供的自动分割的2D叠加(B,E)。在右边(C,F)显示了所得到的三维模型,其中有30个单独标记的骨髓空间。上排,外部测试集I(中心2)的41岁男性多发性骨髓瘤患者的示例图像。下行,外部测试集II中新诊断的多发性骨髓瘤的59岁男性患者(中心8)
本项研究实施了一种深度学习算法,在多中心的数据集中,通过对每个BMS的单独标记实现了从Wb-MRI中进行稳健的自动BM分割。与每个BMS的后续放射组学分析相结合,使传播性BM疾病的自动、全面、客观的BM表型成为可能。这一概念允许从全身成像中自动提取全面的、结构化的数据并用于大规模的研究分析,以实现精确的肿瘤学评估。
原文出处:
Markus Wennmann,André Klein,Fabian Bauer,et al.Combining Deep Learning and Radiomics for Automated, Objective, Comprehensive Bone Marrow Characterization From Whole-Body MRI: A Multicentric Feasibility Study.DOI:10.1097/RLI.0000000000000891


